Ontstekingen, afweerstoornissen, metabole stoornissen
Ontstekingen, afweerstoornissen, metabole stoornissen admin 22 april, 2010 - 10:54Systemische Lupus Erythematosus (SLE)
Systemische Lupus Erythematosus (SLE) fajenn 28 juni, 2010 - 11:53Inleiding
InleidingSLE is de algemeen gebruikelijke aanduiding voor een ziekte van het immuunsysteem (dat is het afweersysteem: de afweer richt zich tegen het eigen lichaam). Veel organen kunnen door de ziekte worden aangetast, ook de hersenen. Zoals vaak bij geneeskundige termen is de naam van de ziekte niet direct inzichtelijk. “Systemische” is afgeleid van het Engelse “systemic” en zou beter vervangen kunnen worden door multi-systemisch of door het in onbruik geraakte “disseminatus” (verspreid). Lupus betekent “wolf” en verwijst naar aantasting van de huid. Erythematosus moet gelezen worden als “met erytheem” (rode verkleuring van de huid). Lupus erythematosus (LE) treft alleen de huid. LE kan overgaan in SLE, een chronische ziekte waarin zich perioden van verslechtering en verbetering voordoen.
Andere teksten op internet
Andere teksten op internetwww.printo.it is de website van de internationale (niet commerciële) organisatie voor onderzoek van proefgeneesmiddelen voor reumatologische ziekten van kinderen, waaronder SLE. De website omvat een uitvoerige, Nederlandstalige beschrijving van SLE bij kinderen
www.kinderneurologie.eu, biedt informatie over uitsluitend de kindervorm van SLE, voor hulpverleners en andere betrokkenen. Verhoudingsgewijze besteedt deze site veel aandacht aan de neurologische kanten van de ziekte
Epidemiologie
EpidemiologieIn Engeland hebben tussen 25 en 90 personen per 100.000 SLE, zeer overwegend vrouwen (verhouding vrouw : man is 9 : 1). Bij Afro-Caraïbische personen komt SLE zevenmaal zo vaak en bij Aziatische personen driemaal zo vaak als bij Indo-Europese (blanke) personen voor (D’Cruz et al. 2007). Overeenkomstige verschillen zijn geconstateerd in de Verenigde Staten van Amerika. Men schat dat SLE in 15 tot 20% van de gevallen debuteert (de eerste verschijnselen geeft) in de kinderjaren (voor de leeftijd van 16 jaar). Niet-blanke (niet-Indo-Europese) kinderen hebben groter risico op de ziekte dan blanke. De kans op de ziekte is veel groter bij meisjes dan bij jongens (±4,5 : 1) (Hiraki et al., 2009; Petty & Laxer, 2005)
Ontstaan
OntstaanDe ziekte SLE
Een aantal factoren bepaalt samen het ontstaan van de ziekte. Zowel erfelijke ontvankelijkheid (aanleg, predispositie) als hormonale factoren en omgevingsfactoren (zoals virale infecties) spelen een rol. Het risico op de ziekte is groter als de aandoening voorkomt bij een eerstegraads familielid. Antilichamen (antistoffen) spelen in het ziekteproces een grote rol. Bij de aanmaak daarvan is een categorie van eenkernige witte bloedcellen betrokken, zogenaamde B lymfocyten.
Hoe ontstaan de ziekteverschijnselen
Verschillende processen bepalen welke verschijnselen zich voordoen (Vermeulen & Huizinga, 2006), bij neurologische of psychiatrische verschijnselen bijvoorbeeld de volgende: 1.Antilichamen tegen hersenweefsel en tegen andere weefsels kunnen functiestoornissen – of functiestoornissen en beschadiging – veroorzaken. 2.Een naar de hersenen toevoerend bloedvat (arterie) kan afgesloten raken door aantasting van de vaatwand of door een bloedstolsel vanuit het hart (embolie). Als gevolg daarvan kan plaatselijk in de hersenen weefselversterf (infarcering) optreden. Ook kan de bloedafvoer uit de hersenen worden belemmerd. 3. Neerslachtigheid of uitgesproken depressie, gepieker en spanningshoofdpijn kunnen als reactie op het hebben van een dergelijke ziekte ontstaan.
Lichamelijke verschijnselen
Lichamelijke verschijnselenDe klachten en verschijnselen verschillen, afhankelijk van de organen die zijn aangetast. Ze variëren in ernst. Klachten over moeheid, jeuk, koorts, veranderingen van de huid en pijn in de gewrichten komen heel veel voor. Kinderen zowel als volwassenen kunnen tijdenlang geheel vrij van verschijnselen (in remissie) zijn, en dan opnieuw verschijnselen krijgen.
Tabel. Lichamelijke verschijnselen van SLE
- Huidaandoening
- rode verkleuring (erytheem), verergerend door zonlicht; in het gelaat heeft de verkleuring veelal de vorm van een over linker- en rechterhelft verdeelde vlinder. Jeuk. Haaruitval
- Nierontsteking
- komt voor bij de meerderheid van de kinderen; mogelijke gevolgen zijn hypertensie, bloedarmoede, oedeem (te veel vocht) onderhuids en niervergiftiging (uraemie)
- Gewrichtsafwijkingen
- pijn en zwelling
- Vaatafwijkingen
- afsluiting van een vat ten gevolge van aantasting van de vaatwand door antilichamen of ten gevolge van ontsteking van de vaatwand
- Neurologisch/psychiatrisch
- epilepsie, depressiviteit, hoofdpijn, gepieker, cognitieve functiestoornis, psychose;
zelden: door herseninfarct veroorzaakte verlamming, hersenvliesontsteking, bewegingsstoornis (chorea), vermindering van gezichtsvermogen, verlamming van de benen door aantasting van het ruggenmerg - Zweertjes (ulceraties) in de mond
- Hartspierontsteking
- Ontsteking van vliezen rond hart en longen
- Bloedarmoede
- Oogafwijkingen
- Aandoeningen van andere organen
Psychiatrische verschijnselen
Psychiatrische verschijnselenEen minderheid van de kinderen met SLE maakt een psychose door; deze kinderen lijden gedurende een periode aan miskenning van de omringende werkelijkheid, met hallucinaties (zinsbedrog, bijvoorbeeld zien van beelden die er in werkelijkheid niet zijn) en soms waanachtige denkbeelden. De psychose is een onmiskenbaar teken van een hersenaandoening. Sommige kinderen, onder andere kinderen met epilepsie, piekeren veel; zij maken zich overmatig bezorgd over reële of ingebeelde gevaren. Veel kinderen maken perioden door van depressieve gestemdheid, al dan niet als reactie op hun chronisch onwel zijn. Het staat vast dat al deze verschijnselen veroorzaakt kunnen worden door de SLE, maar dat behoeft zorgvuldige diagnostiek want ze kunnen ook andere oorzaken hebben (Mina & Brunner, 2010).
Stoornissen van het cognitieve functioneren
Stoornissen van het cognitieve functionerenDe gangbare opvatting was dat veel kinderen met SLE cognitieve functiestoornissen hadden. Verschillende onderzoekers hadden dergelijke stoornissen gerapporteerd bij 5 tot 59 procent van de kinderen (Sibbitt et al., 2002; Harel et al., 2006; Brunner et al., 2007). De verklaring voor de enorme verschillen in percentages was onzeker (Mina & Brunner, 2010). Bijna alle tot voor kort beschikbare informatie was retrospectief (achteraf) verzameld, een veel minder betrouwbare procedure dan prospectieve (van te voren geplande) verzameling.
Van belang is dat cognitieve functiestoornissen waarschijnlijk meer voorkomen bij Afro-Amerikaanse en Afro-Caraïbische kinderen dan bij Indo-Europese (blanke) kinderen en meer bij kinderen in de eerste twee jaren na debuut van de ziekte dan later (Brunner et al, 2007). Onzeker is hoe lang cognitieve stoornissen aanhouden.
Intelligentieonderzoek in kleine groepen kinderen (te klein om algemene conclusies op te baseren) leverde een gemiddeld laag normaal tot normaal (≥ 85) totaal Intelligentiequotiënt (IQ) op (Wyckoff et al. 1995; Jennekens-Schinkel & Jennekens, 2008). Over stoornissen van taal, geheugen en leren konden geen op onderzoek berustende uitspraken worden gedaan. Klachten over aandacht en concentratie schenen veel voor te komen (Jennekens-Schinkel & Jennekens, 2008).
In het eerste onderzoek dat wel prospectief was opgezet werden 41 kinderen met SLE en 22, wat geslacht, leeftijd en etniciteit betreft vergelijkbare controle kinderen neuropsychologisch onderzocht. Er waren wel cognitieve functiestoornissen maar deze verschilden niet in de twee groepen (Williams et al. 2011). Dit resultaat werd in 2012 bevestigd in een onderzoek van 40 SLE kinderen en 40 nauwkeurig vergelijkbare (geslacht, leeftijd, etniciteit, opleiding van de moeder, familie inkomen) controle kinderen (Zelko et al. 2012). Over de activiteit van de SLE ten tijde van deze twee prospectieve onderzoekingen is geen informatie verstrekt; mogelijk was de SLE bij allen in remissie.
Dergelijke toch nog kleine onderzoeksgroepen sluiten lichte en voorbijgaande ernstiger cognitieve stoornissen niet uit, maar dat ernstige, aanhoudende cognitieve stoornissen veel voorkomen, is niet aannemelijk.
Diagnose
DiagnoseDe diagnose SLE wordt gesteld op grond van een combinatie van bevindingen (ziekteverschijnselen en laboratoriumafwijkingen). Overleg van deskundigen heeft geleid tot overeenstemming over 11 criteria die elk passen bij de diagnose. Drie criteria hebben betrekking op huidafwijkingen en twee op immunologische afwijkingen (aanwezigheid van verschillende antilichamen) in het bloed. Aanwezigheid van één of meer neurologische of psychiatrische afwijkingen telt ook als criterium. Men kan tot SLE besluiten wanneer aan vier van de 11 criteria gelijktijdig of na elkaar is voldaan. De mate van activiteit van het ziekteproces kan zowel gedurende het beloop van de ziekte als tussen kinderen of jongeren met de ziekte sterk uiteen lopen.
Medische behandeling
Medische behandelingKinderen moeten hun conditie op peil houden en, bij overgevoeligheid voor licht, zonlicht vermijden. Ter vermindering van de activiteit van de ziekte worden middelen voorgeschreven die ontsteking remmen (zoals prednison) en afweerreacties onderdrukken. Een nieuwe behandelingswijze is het selectief verminderen van het aantal B lymfocyten met een daarvoor geschikt bevonden geneesmiddel (Rituximab) (Podolskaya et al., 2008). Afhankelijk van de verschijnselen kunnen andere geneesmiddelen worden voorgeschreven, bijvoorbeeld bloeddrukverlagende middelen bij hypertensie, een bloedverdunnend middel bij risico op dichtslibben van een vat, anti-epileptica in geval van epilepsie, een antidepressivum bij depressie, enz.
Beloop
BeloopBeoordelingslijsten waarop de ziekteactiviteit van SLE wordt uitgedrukt in schaalwaarden tonen aan dat kinderen zeker in de beginperiode flink ziek zijn, verhoudingsgewijze ernstiger dan volwassenen (Brunner et al., 2008). De kinderen worden veelal behandeld met hoge doseringen prednison, en tegenwoordig ook met middelen die het aantal B lymfocyten en de productie van antilichamen verminderen. Het gunstige gevolg hiervan is dat de ziekteactiviteit vermindert. Nog maar weinig kinderen overlijden door SLE. Tot voor kort hield de helft van de kinderen wel blijvende nadelige gevolgen. Zo kan de SLE leiden tot een gestoorde nierfunctie. De prednisonbehandeling kan staar, striae (streepvormige verdunning van de huid) en botafwijkingen (osteoporose) ten gevolge hebben. Betreffende het cognitieve functioneren op lange termijn is nog weinig met zekerheid bekend, maar ernstige functiestoornissen zijn niet gerapporteerd. Geneeskundige controle blijft, ook als het beloop gunstig is, nodig omdat de ziekte weer kan verergeren.
Psychosociaal functioneren
Psychosociaal functionerenHet psychosociale functioneren kan door een veelheid van factoren beperkt worden (Jennekens-Schinkel & Jennekens, 2008). Kinderen met SLE zijn in variabele mate onwel. Ze zijn vaak moe ten gevolge van bloedarmoede, ontstekingen, overbelasting en andere oorzaken; ze kunnen in beslag genomen zijn door pijn, bijvoorbeeld hoofdpijn of gewrichtspijn; ze kunnen gehinderd worden door jeuk ten gevolge van hun huidaandoening. Bij overgevoeligheid voor zonlicht worden ze beperkt in hun mogelijkheden om mee te doen met leeftijdsgenoten. De rode verkleuring van de huid, in onder meer het gelaat, kan aanleiding geven tot gevoelens van verlegenheid of schaamte, hetzelfde geldt voor overmatige haaruitval. Ook epileptische aanvallen kunnen gevoelens van schaamte oproepen. De intrede van de puberteit kan door SLE vertraagd zijn. De maandelijkse bloedingen kunnen onregelmatig zijn. Bij behandeling met prednison worden de kinderen bedreigd door overmatige toename van gewicht, waardoor kinderen zich nog meer voor hun uiterlijk kunnen schamen en waardoor op school pesterij kan worden uitgelokt. Andere sociaal nadelige effecten van prednisonbehandeling kunnen zijn: versterkte haargroei op plaatsen waar dat onwenselijk is, striae die zichtbaar worden in badkleding, vertraagde groei. En tenslotte, kinderen met SLE gaan meer dan anderen een onzekere toekomst tegemoet (Kone-Paut et al., 2007).
Schoolloopbaan veelal belemmerd
De vorderingen op school zijn volgens beoordelingen door ouders bij kinderen met SLE minder dan bij goed vergelijkbare controle kinderen (Zelko et al. 2012). Duidelijk is dat het onwelzijn, mogelijke, voorbijgaande cognitieve functiestoornissen en psychiatrische problemen, het met dit alles samenhangende schoolverzuim en tenslotte de psychosociale problemen, samen een groot risico kunnen vormen voor de prestaties op school. Sommige jongeren met SLE kiezen een vervolgopleiding onder hun intellectuele mogelijkheden, om minder kans te hebben op falen door de energetische, pijn- en andere problemen en het in fasen van verergering vele ziekenhuisbezoek - en dus schoolverzuim.
Begeleiding
Begeleiding- Ervaringsgegevens wijzen uit dat kinderen op basis van goede informatie over hun kwaal in staat zijn hun ziek zijn te accepteren, controle te houden over hun leven en verantwoordelijkheid te nemen voor het gebruik van geneesmiddelen
- Behoud van sociale integratie is daarbij van groot belang: op school, in de woonomgeving, voorzover mogelijk bij sport, en bij spel (Moorthy et al., 2007).
- in geval van problemen bij het verwerven van schoolvaardigheden, of in de schoolloopbaan, kan neuropsychologisch onderzoek behulpzaam zijn bij het identificeren van de oorzaak
- De overgang van kinderarts naar reumatoloog is voor de adolescent van cruciaal belang. Zorgvuldige voorbereiding, inclusief heldere voorlichting, kan voorkomen dat de jongere zich aan medische controle en behandeling onttrekt.
Een kind met SLE
Een kind met SLE fajenn 29 juni, 2010 - 12:12Literatuur
LiteratuurBrunner HI, Ruth NM, German A, Nelson S, Passo MH, Roebuck-Specer T, Ying J, Ris D (2007) Initial validation of the Pediatric automated neuropsychological assessment metrics for childhood-onset systemic lupus erythematosus. Atrhritis & Rheumatism 57: 1174-1182
Brunner HI, Gladman DD, Ibanez D, Urowitz MD, Silverman ED (2008) Difference in disease features between childhood-onset and adult-onset systemic lupus erythematosus. Arthritis & Rheumatism 58: 556-562
D’Cruz DP, Khamashta M, Hughes GR (2007) Systemic lupus erythematosus. The Lancet 369: 587-596
Harel L, Sandborg C, Lee T, Scheven E von (2006) Neuropsychiatric manifestations in pediatric systemic lupus erythematosus and association with antiphospholipid antibodies The Journal of Rheumatology 33: 1873-1877
Hiraki LT, Benseler SM, Tyrrell PN, Harvey E, Hebert D, Silverman ED (2009) Ethnic differences in pediatric systemic lupus erythematosus. Journal of Rheumatology 36: 2539-2546
Jennekens-Schinkel A, Jennekens FGI (2008) Neuropsychologie van neurologische aandoeningen in de kindertijd. Amsterdam: Boom, pp 547-564
Kone-Paut I, Piram M, Guillaume S, Tran TA (2007) Lupus in adolescence. Lupus 2007; 16: 606-612
Mina R, Brunner HI (2010) Pediatric lupus - are there differences in presentation, genetics, response to therapy, and damage accrual compared with adult lupus. Rhematic Diseases Clinic North America 36: 53-80
Moorthy LN, Peterson MGE, Baratelli M, Harrison MJ, Onel KB, Chalom EC, Haines K, Hashkes PJ, Lehman TJA (2007) Multicenter validation of a new quality of life measure in pediatric lupus. Arthritis & Rheumatism 57: 1165-1173
Petty RE, Laxer RM (2005) Systemic lupus erythematosus. In: Cassidy JT, Petty RE, Laxer RM, Lindsey CB (redacteuren) Textbook of Pediatric Rheumatology. Amsterdam: Elsevier Saunders, hoofdstuk 16, pp 342-385
Podolskaya A, Stadermann M, Pilkington C, Marks SD, Tullus K (2008) B cell depletion therapy for 19 patients with refractory systemic lupus erythematosus. Archives of Disease in Childhood 93: 401-406
Sibbitt WL Jr, Brandt JR, Johnson CR, Maldonado ME, Patel SR, Ford CC, Bankhurst AD, Brooks WM (2002) The incidence and prevalence of neuropsychiatric syndromes in pediatric onset systemic lupus eryhtematosus. The Journal of Rheumatology 29: 1536-1542
Vermeulen M, Huizinga TWJ (2006) Neurologische of psychiatrische symptomen bij patienten met lupus erythematodes disseminatus (SLE): terminologische problemen, pathogenese, diagnostiek en therapie. Nederlands Tijdschrift voor Geneeskunde 150: 367-372
Williams TS, Aranow C, Ross GS, Barsdorf LS, Imundo LF, Eichenfeld AH et al. (2011) Neurocognitive impairment in childhood-onset systemic lupus erythematosus: measurement issues in diagnosis. Arthritis Care & Research (Hoboken) 63: 1178-1187
Wyckoff PM, Miller LC, Tucker LB, Schaller JG (1995) Neuropsychological assessment of children and adolescents with systemic lupus erythematosus. Lupus 4: 217-220
Zelko F en 9 anderen, laatste auteur Brunner HI (2012) Academic outcomes in childhood-onset systemic lupus erythematosus. Arthritis Care & Research 64: 1167 - 1174
Narcolepsie
Narcolepsie fajenn 21 maart, 2012 - 15:57Inleiding
InleidingMet het woord narcose wordt voorbijgaande bewusteloosheid aangeduid; lepsis staat voor aanval. De term narcolepsie wordt gebruikt voor een syndroom waarvan excessieve slaapzucht overdag met onweerstaanbare slaapaanvallen de kernverschijnselen zijn. Narcolepsie is een blijvende invaliderende aandoening.
Men onderscheidt 3 vormen:
1. Narcolepsie met kataplexie
2. Narcolepsie zonder kataplexie
3. Narcolepsie als gevolg van andere medische aandoeningen
De term kataplexie komt van het Grieks: "kata" betekent "omlaag" en "plexis" betekent "treffen". Kataplexie duidt plotseling, kort verlies van spiertonus aan.
Na vermelding van geselecteerde andere teksten op internet en van epidemiologische gegevens, zullen we de mogelijke oorzaken bespreken en de lichamelijke verschijnselen beschrijven en daarna ingaan op de psychosociale problemen van kinderen met dit syndroom.
Andere teksten op internet
Andere teksten op internet• www.kinderneurologie.eu: de informatie over narcolepsie op deze website betreft overwegend de medische aspecten. De tekst is geschreven door een kinderneuroloog.
• Zoek op internet naar “Narcolepsie, diagnostiek en behandeling in nieuw perspectief” . Men vindt dan een artikel over dit onderwerp dat gepubliceerd is in het Nederlands Tijdschrift voor Geneeskunde door R Fronczek en anderen (2006) maar dat niet vrij toegankelijk is, alsmede een hoofdstuk uit een boek gebaseerd op dit artikel dat wel vrij toegankelijk is. Zoekt men naar "Fronczek en narcolepsie" dan vindt men de samenvatting van het proefschrift van Dr Fronczek over Narcolepsie.
Epidemiologie
EpidemiologieIn 2007 waren in Nederland naar schatting 1000 patiënten bekend, (kinderen, adolescenten en volwassenen, meisjes en jongens) (Fronczek et al., 2007). Gegeven de cijfers over de prevalentie in andere Europese landen (20-50 per 100.000) zou men voor Nederland ongeveer 7000 patiënten met narcolepsie verwachten.
De incidentie bedraagt (in Minnesota, USA) ongeveer 2 per 100.000 en is het hoogste tussen het tiende en twintigste levensjaar. Ook bij kinderen jonger dan 10 jaar kan narcolepsie ontstaan (zie Akintomide en Rickards, 2010).
Bij familieleden van kinderen met narcolepsie doet de aandoening zich meer voor dan verklaarbaar door toeval, het geen wijst op een genetische factor in het mechanisme van ontstaan van de ziekte. Familiair voorkomen van narcolepsie met kataplexie is bekend maar is zeldzaam (Hor et al., 2011)
Oorzaken van narcolepsie
Oorzaken van narcolepsie1. Hypocretinedeficiëntie
Narcolepsie met kataplexie is in de regel het gevolg van een tekort (deficiëntie) in hypocretine. Hypocretine 1 en hypocretine 2 zijn verwante neuropeptiden die aangemaakt worden door zenuwcellen in het bovenste laterale deel van de hypothalamus (zie ook ENCYCL-Anatomie van de hersenen). Men neemt aan dat de hypocretinen neurotransmittors zijn. Hypocretine-neuronen sturen axonen uit naar zenuwcellen in verschillende delen van de hersenstam (zie ook ENCYCL-Anatomie van de hersenen en in de grote hersenen. Hypocretineneuronen worden verondersteld de “waaktoestand” te ondersteunen, betrokken te zijn bij de regulering van het slaap-waak ritme en de zogeheten REM-slaap te onderdrukken. Ze spelen een rol bij verschillende andere functies, waaronder die van voeding en verslaving (Kornum et al., 2011).
Normaliter is hypocretine aantoonbaar in de liquor cerebrospinalis, maar in de liquor cerebrospinalis van mensen met narcolepsie en kataplexie is dit neuropeptide in sterk verminderde mate of niet aanwezig. Dankzij onderzoek van het hersenweefsel van overledenen met narcolepsie en kataplexie is ontdekt dat de hypocretineneuronen in de hypothalamus geheel of grotendeels zijn verdwenen en vervangen door gewoekerde gliacellen. Nabijgelegen andere neuronen zijn normaal aanwezig. Een dergelijke selectieve uitval zou verklaard kunnen worden door een auto-immuunreactie, bijvoorbeeld door een antistof tegen een antigeen aan het oppervlak van hypocretineneuronen. Deze veronderstelling wordt algemeen aannemelijk geacht. De gangbare auto-immuun therapieën (behandeling met corticosteroïden of immuunglobulinen) hebben echter bij narcolepsie met kataplexie geen of geen duidelijk effect (Kornum et al., 2011; Cvetkovic-Lopes et al., 2010).
Ook sommige mensen met narcolepsie zonder kataplexie hebben te weinig hypocretine in de liquor. Mogelijk zal de kataplexie bij hen nog ontstaan als de afbraak van hyporetineneuronen voortschrijdt.
Uitval van hypocretineneuronen in de hypothalamus en overmatige slaperigheid overdag komen ook voor bij de ziekte van Alzheimer (Fronczek et al., 2011 ).
2.Een genetische afwijking
Onlangs is voor het eerst een genetische afwijking (een “missense mutatie ” in het glycoproteïne van oligodendrocyten) (zie ook ENCYCL-Anatomie van de hersenen) aangetoond bij een familiaire vorm van narcolepsie met kataplexie (Hor et al., 2011).
3.Idiopathisch
Bij de meeste kinderen en adolescenten met narcolepsie zonder kataplexie wordt geen duidelijke oorzaak gevonden. Kataplexie zou, althans bij een aantal van hen, later kunnen ontstaan.
Lichamelijke verschijnselen
Lichamelijke verschijnselenNarcolepsie
Overmatige slaperigheid overdag en kortdurende onweerstaanbare slaapaanvallen overdag vormen de kernverschijnselen van narcolepsie. De dagelijks aanwezige overmatige slaperigheid leidt tot tekorten in opmerkzaamheid (vigilantie) en tot het min of meer automatisch verrichten van handelingen waardoor fouten gemaakt worden. De slaapaanvallen treden vooral op als bijzondere oplettendheid niet vereist is, zoals bij welbekende routine handelingen. Na het slapen voelen de patiënten zich verfrist. ’s Nachts wordt men vaker dan gebruikelijk wakker (gefragmenteerde slaap). Narcolepsie begint als regel met overmatige slaperigheid overdag. Kataplexie is vanaf het begin aanwezig of volgt na kortere of langere tijd (Fronczek et al., 2007).
Kataplexie
Plotseling verlies van spierspanning (tonus) kan zich in bepaalde spieren, symmetrisch, of asymmetrisch, in een deel van het lichaam of gegeneraliseerd voordoen (Overeem et al., 2011). Vooral partieel tonus verlies duurt kort: naar schatting vaak minder dan 10 seconden. Gegeneraliseerd tonusverlies duurt langer: soms minuten. We noemen een viertal voorbeelden van partieel verlies van spiertonus: slapte in het gezicht, slapte van de kaakspieren waardoor de mond gaat open hangen, slapte van de halsspieren waardoor het hoofd voorovervalt, en slapte van de kniestrekkers waardoor men kan vallen. Bij gegeneraliseerde aanvallen zakken patiënten ineen en kunnen zich enkele ogenblikken niet bewegen. Men voelt gegeneraliseerde aanvallen vaak aankomen, bijvoorbeeld door partiële zwakte of door een vreemd gevoel in het hoofd. Het bewustzijn blijft helder. Tot groot letsel leidt het vallen doorgaans niet maar blauwe plekken en schrammen zijn geen zeldzaamheid en bij uitzondering doen zich gevaarlijke situaties voor. De spiertonus herstelt plotseling. De aanvallen treden vooral (maar niet uitsluitend) op bij emoties, zoals bij intens lachen en bij boosheid. De aanvallen kunnen sporadisch maar soms ook vele malen per dag voorkomen.
Andere verschijnselen
Hypnagoge hallucinaties, slaapparalyse en gefragmenteerde nachtrust komen zowel bij narcolepsie met kataplexie als bij andere vormen van overmatige slaperigheid overdag voor. Ze zijn daarom niet van belang voor de diagnostiek van narcolepsie. Ze zijn bij narcolepsie ook niet altijd aanwezig.
• Hallucinaties die zich tijdens inslapen of wakker worden voordoen worden hypnagoog genoemd. Het zijn droomachtige ogenschijnlijk realistische, soms beangstigende ervaringen.
• Kortdurend niet kunnen bewegen tijdens wakker worden of inslapen wordt aangeduid als slaapparalyse.
• De nachtrust is gefragmenteerd als de slaper veelvuldig ontwaakt en enige tijd wakker blijft.
• Voor de diagnose narcolepsie is nodig dat andere oorzaken voor overmatige slaperigheid overdag ontbreken (Fronczek et a., 2007).
Voor de diagnose narcolepsie is nodig dat andere oorzaken voor overmatige slaperigheid overdag ontbreken (Fronczek et al., 2007)
Diagnostische criteria volgens de “International Classifiucation of Sleep Disorders”(Akintomide & Rickards, 2011)
1.Narcolepsie met kataplexie
- Overmatige slaperigheid overdag sinds tenminste 3 maanden
- Overtuigende beschrijving van kortdurende aanvallen van tonusverlies
- De zogeheten *Multipele inslaaplatentietest (MSLT) toont een gemiddelde slaaplatentietijd van minder dan 8 minuten, waarbij tenminste tweemaal bij 5 keer inslapen REM-slaap aanwezig is.
- Hypocretine spiegel in de liquor is hooguit 110 picrogram per milliliter, of minder dan 1/3de van normaal.
- Hypersomnie kan niet beter op andere wijze worden verklaard
2.Narcolepsie zonder kataplexie
- Overmatige slaperigheid overdag sinds tenminste 3 maanden
- MSLT: gemiddelde inslaaptijd bij 5 keer inslapen minder dan 8 minuten, in 2 van 5 gevallen met REM-slaap bij inslapen.
- Hypersomnie kan niet beter op andere wijze worden verklaard.
3. Narcolepsie secundair aan een andere medische aandoening
- Overmatige slaperigheid overdag sinds tenminste 3 maanden
- Kataplexie is aanwezig
- Bij ontbreken van kataplexie moet de gemiddelde slaaplatentietijd worden onderzocht en moet bij inslapen REM-slaap optreden.
- Hypocretine-spiegel in de liquor is minder dan 110 picrogram per milliliter
- Er is een andere medische aandoening die de narcolepsie voldoende verklaart, bijvoorbeeld de ziekte van Alzheimer
- Hypersomnie kan niet verklaard worden door een andere aandoening dan narcolepsie.
*De Multipele Slaaplatentietest omvat het volgende: men laat onderzochte vijfmaal op een dag in bed liggen in een donkere kamer en meet de tijd tot inslapen. Als bevestiging van de diagnose narcolepsie gelden: een gemiddelde slaaplatentietijd van 8 minuten of minder en tenminste twee maal REM-slaap kort na het inslapen.
Co-morbiditeit
Co-morbiditeitAssociaties met andere aandoeningen komen voor zover bekend niet overtuigend voor (Stores et al;., 2006). De indruk bestaat dat mensen met narcolepsie en kataplexie vaak zwaarlijvig zijn. Onduidelijk is of dat ook geldt voor kinderen en adolescenten (K&A).
Cognitie
CognitieDe intelligentie van kinderen en adolescenten met narcolepsie ligt over het algemeen in het gemiddelde gebied, het geen wil zeggen dat het intelligentiequotiënt ergens tussen 90 en 110 ligt (een IQ van 100 is precies gemiddeld). Tussen de verbale en performale componenten van het IQ lijkt bij meer kinderen dan normaal een discrepantie voor te komen (Dorris et al., 2008). Bij sommigen is het verbale IQ beter en bij andere het performale. Bij volwassenen lijkt de inspanning waakzaam te blijven ten koste te gaan van de uitvoering van cognitieve taken waarin controle een belangrijk aspect is (Naumann et al., 2006).
Psychosociale problemen
Psychosociale problemenOp school hebben kinderen en adolescenten met narcolepsie en kataplexie meer gedragsproblemen; ze zijn minder opgewekt dan andere kinderen. Ouders beoordelen de kwaliteit van deze kinderen als verminderd (Stores et al., 2006). De kinderen verschillen in deze opzichten weinig of niet van kinderen en adolescenten met overmatige slaperigheid overdag zonder kataplexie. Verondersteld wordt daarom dat de psychosociale problemen geen verschijnsel zijn van de narcolepsie maar een gevolg van de overmatige slaperigheid.
Deze uitspraken steunen op een enkel, internationaal onderzoek waarin 42 kinderen en adolescenten met narcolepsie en kataplexie (gemiddelde leeftijd 12 jaar) en 18 kinderen met overmatige slaperigheid overdag (gemiddelde leeftijd 14 jaar) vergeleken werden met 23 controlekinderen zonder slaapproblemen (gemiddelde leeftijd 14 jaar) (Stores et al., 2006). Niemand was ouder dan 18 jaar. De gegevens werden verkregen met behulp van vragenlijsten. Ze worden hier vrij uitvoerig gerapporteerd omdat ander onderzoek ontbreekt.
- Blijkens de Strength and Difficulty Questionaire (SDQ). Groepsgewijze hadden beide groepen kinderen en adolescenten met slaapproblemen meer ongewenst gedrag, meer moeilijkheden met leeftijdsgenoten en meer tekenen van emotionele problemen. Ook hadden ze meer negatieve invloed op het gezinsleven. Hyperactiviteit kwam bij hen niet meer voor dan bij controles en dan bij kinderen in het algemeen.
- In de beide groepen kinderen met slaapproblemen bestonden volgens de Child Depression Inventory (CDI) aanzienlijk meer aanwijzingen voor depressie dan bij de controlekinderen (maar die hadden wel opvallend veel minder tekenen van depressie dan in de algemene kinderbevolking). Verhoogde tekenen van depressiviteit bleken ook uit de beoordelingen van de ouders op de Child Health Questionaire (CHQ).
- Kinderen en adolescenten met narcolepsie en kataplexie verzuimden niet buitensporig veel maar hun schoolvorderingen bleven achter ondanks vaak extra inspanning van de leerkracht. Inzicht in de achtergronden daarvan werd belemmerd door gebrek aan medewerking van leerkrachten.
De moeite die de auteurs zich moesten getroosten om kinderen met beide soorten slaapstoornis te bereiken voor hun onderzoek doet vermoeden dat de symptomen vaak langdurig worden miskend, met de nodige negatieve gevolgen voor de ontwikkeling van de kinderen (Stores et al., 2006; zie ook Overeem et al., 2011).
Medische behandeling, Psychologische-Pedagogische begeleiding
Medische behandeling, Psychologische-Pedagogische begeleidingGeneesmiddelen hebben effect maar voorkomen of onderdrukken de verschijnselen niet volledig.
1. Modafinil verbetert overmatige slaperigheid overdag bij myotone dystrofie en is het middel van eerste keuze bij narcolepsie.
2. Methylphenidaat is bekend vanwege het gunstige effect op aandacht en hyperactiviteit bij kinderen met ADHD en wordt ook gebruikt voor het verminderen van excessieve slaperigheid overdag bij narcolepsie.
3. Een geneesmiddel voor selectieve behandeling van kataplexie is niet bekend.
4. Gammahydroxyboterzuur (merknaam Xyrem) is zowel effectief voor kataplexie, als voor overmatige slaperigheid overdag en verbetering van nachtrust. De toediening is complex en het middel is niet zonder bijwerkingen (Akintomide en Rickards, 2011). Om een optimaal resultaat te bereiken is advies van een specialist met ervaring op dit gebied aan te bevelen (zie Lammers et al. , 2010, met antwoord van Zvosec et al., 2010). Vanwege een mogelijk nadelig effect op de nachtelijke ademhaling wordt incidentele controle van nachtelijke zuurstofwaarden aanbevolen.
Schoolomstandigheden Onderzoekgegevens over optimale schoolomstandigheden voor kinderen met deze handicap ontbreken. Leerkrachten van welke school ook, hebben in de regel geen kennis over narcolepsie; zij behoeven deskundige voorlichting. Medeleerlingen moeten weten dat slaapstoornissen het gevolg van een hersenaandoening kunnen zijn. Kinderen en adolescenten met narcolepsie functioneren beter als in hun schoolrooster op gezette tijdstippen korte slaappauzes worden ingelast (Akintomide & Rickards, 2011) .
Centra voor slaapstoornissen De meeste kennis over slaapstoornissen bij kinderen en adolescenten is aanwezig in centra voor slaap en waakstoornissen. De website van de Nederlandse Vereniging voor Narcolepsie (www.narcolepsie.nl ) vermeldt 9 slaap centra genoemd, 3 in Overijsel, 2 in Amsterdam, en 1 in de gemeenten, Den Haag, Heeze, Leiden en Sittard. De neurologen van het Leids Universitair Medisch Centrum (LUMC) den kunnen door hun jarenlang onderzoek bogen op veel kennis en ervaring.
Medewerkers van het “ Expertisecentrum voor Epileptologie, Slaapgeneeskunde en Neurocognitie" in Kempenhaeghe (Heeze) zetten zich onder andere in voor begeleiding en onderwijs van kinderen en adolescenten met narcolepsie.
Een kind met narcolepsie
Een kind met narcolepsie fajenn 13 april, 2012 - 09:53Literatuur
LiteratuurAkintomide GS, Rickards H (2011) Narcolepsy: a review. Neuropsychiatric Disease and Treatment 7: 507-518
Cvetkovic-Lopes V en 14 anderen (2010) Elevated Tribbels homolog 2-specific antibody levels in narcolepsy patients. The Journal of Clinical Investigation 120: 713-719
Dorris L, Zuberi SM, Scott N, Moffat C, McArthur I (2008) Psychosocial and intellectual functioning in childhood narcolepsy. Developmental Neurorehabilitation 11: 187-194
Fronczek R, van Geest S, Frölich M, Overeem S, Roelandse FW, Lammers GJ, Swaab DF (2011) Hypocretin (orexin) loss in Alzheimer’s disease. Neurobiology Aging, Epub May 3á
Fronczek R, van der Zande WLM, van Dijk JG, Overeem S, Lammers GJ (2007) Narcolepsie : diagnostiek en behandeling in nieuw perspectief. Nederlands Tijdschrift voor Geneeskunde 151; 856-861
Hor H, Bartesaghi L, Kutalik Z, Vicário JL, de AndréThe s C, Pfister C, Lammers GJ, Guex N Chrast R , Tafti M, Peraita-Adrados R (2011) A missence mutation in myelin oligodendrocyte glycoprotein as a cause of familial narcolepsy with cataplexy. The American Journal of Human Genetics 89: 474 - 479
Kornum BR, Faraco J, Migriot E (2011) Narcolepsy with hyocretin/orexin deficiency, infections and autoimmunity of the brain. Current Opinion in Neurobiology 21: 1-7
Lammers GJ en 24 anderen (2010) Sodium oxybate is an effective and safe treatment for narcolepsy. Response from Zvosec DL, Smith SW, Hall BJ. Sleep Medicine 11: 105-109
Naumann A, Bellebaum C, Daum I (2006) Cognitive deficits in narcolepsy. Journal of Sleep Research 15: 329-338
Overeem S, van Nues SJ, van der Zande WL, Donjacour CE, van Mierlo P, Lammers GJ (2011) The clinical features of cataplexy: a questionnaire study in narcolepsy patients with and without hypocretin1 deficiency. Sleep Medicine 12: 12-18
Stores G, Montgomery P, Wiggs L (2006) The psychosocial problems of children with narcolepsy and those with excessive daytime sleepiness of uncertain origin. Pediatrics 118: e1116- 1123
Bacteriële meningitis
Bacteriële meningitis fajenn 30 juni, 2010 - 16:19Inleiding
InleidingHersenen en ruggenmerg worden omgeven door drie vliezen, de meningen. De dura mater is een stevig vlies dat direct onder de schedel ligt. De arachnoïdea is veel dunner dan de dura mater, dit middelste vlies ligt tegen de dura aan en kan er langs glijden. De pia mater, het binnenste van de drie vliezen, ligt tegen hersenen en ruggenmerg en volgt de contouren daarvan. Arachnoïdea en pia mater zijn door vezelige bindweefselstrengen met elkaar verbonden.
In de ruimte tussen arachnoidea en pia mater bevindt zich de liquor cerebrospinalis. In deze “liquorruimte” kan zich ontsteking (hersenvliesontsteking of meningitis) voordoen en verspreiden. Meningitis ontstaat meestal doordat ziektekiemen zoals bacteriën, virus of schimmels de liquorruimte binnendringen. Bacteriën zijn eencellige micro-organismen zonder celkern van 0,1- 10 µm die alles in zich hebben om te overleven. Virus zijn niet veel meer dan erfelijk materiaal in de vorm van RNA of DNA met daaromheen een eiwitmantel. Ze kunnen zich alleen intracellulair vermeerderen. Virale meningitis heeft geen cognitieve gevolgen. Meningitis door schimmelinfecties is bij kinderen in Nederland uitzonderlijk. Tuberculose, syfilis en de ziekte van Lyme zijn bacteriële ontstekingen maar worden niet tot de “gewone bacteriële aandoeningen” gerekend. Meningitiden door tuberculose of syfilis kunnen wel cognitieve gevolgen hebben maar komen in Nederland bij kinderen gelukkig zeer weinig voor. Meningitis door de ziekte van Lyme (overgebracht via een tekenbeet) is niet zeldzaam; het is een goed behandelbare aandoening die geneest zonder nadelige gevolgen voor het cognitieve functioneren. Deze drie bacteriële meningitiden blijven hier buiten beschouwing. Bij pasgeborenen en jonge kinderen zijn streptokokken, meningokokken, pneumokokken en coli bacteriën de meest voorkomende verwekkers van bacteriële meningitis. Dankzij vaccinatie komt meningitis door haemophilus influenza b in Nederland bijna niet meer voor.
Andere teksten op internet
Andere teksten op internetwww.kinderneurologie.eu geeft een goed overzicht van de medische aspecten van hersenvliesontsteking. De tekst is bestemd voor hulpverleners en familieleden.
www.neurologie.nl/files geeft toegang tot een Richtlijn voor artsen over Bacteriële meningitis die dateert van 2013.
Epidemiologie
EpidemiologieIn 2003 werden in Nederland in de leeftijdscategorie jonger dan vijf jaar 233 kinderen geregistreerd met bacteriële meningitis (www.nationaalkompas.nl). Door verbeterde vaccinatie is het aantal gevallen in die leeftijdscategorie gedaald tot 68 in 2013. Van de kinderen die bacteriële meningitis doormaken tussen 0 en 10 jaar stierf tot enkele jaren geleden 2,5% (Koomen, 2003).
Oorzaken
OorzakenBacteriën kunnen de liquorruimte binnendringen vanuit het bloed, vanuit een nabijgelegen ruimte zoals bijvoorbeeld een neusbijholte of het middenoor. Tijdens de geboorte kan de boreling besmet worden in het geboortekanaal. Kinderen kunnen besmet worden via ophoesten door een ander persoon, waarbij besmette druppeltjes terecht komen in de neuskeelholte van het kind. Meningitis gaat bij een grote minderheid van de kinderen gepaard met sepsis (Roos, 1997).
De ontsteking in de liquorruimte kan passerende of nabijgelegen bloedvaten doen ontsteken en verstoppen waardoor de bloedvoorziening van hersenweefsel plaatselijk kan tekortschieten waardoor daar een infarct kan ontstaan. Ook kunnen zenuwen worden aangetast die de liquorruimte passeren op hun baan van de hersenen naar nabijgelegen weefsel zoals oogspieren; daardoor kan bijvoorbeeld oogspierverlamming ontstaan. De ontsteking in de liquorruimte kan het nabijgelegen hersenweefsel vochtrijk maken en doen ontsteken. De ontsteking kan de cochlea aantasten en daar resulteren in bindweefselvorming.
Lichamelijke stoornissen
Lichamelijke stoornissenVerschijnselen
Deze zijn anders bij pasgeborenen dan bij oudere kinderen.
- De baby is prikkelbaar, de voeding verloopt met moeite, de lichaamstemperatuur is te hoog of te laag, de ademhaling is versneld, het bewustzijn is veranderd en soms zijn er epileptische aanvalletjes.
- Bij het wat oudere kind wijzen de verschijnselen duidelijker op de onderliggende oorzaak. Het kind heeft hoofdpijn, het is onwel, het heeft koorts, het kan gaan ijlen; het bewustzijn daalt en er zijn epileptische aanvallen. Bij onderzoek kan blijken dat het een stijve nek heeft en dat ter plaatse van de fontanellen het onderhuidse tussenliggende vlies ongewoon gespannen is.
Bij kinderen met meningokokkenmeningitis kunnen bloedinkjes in de huid een teken zijn van sepsis. Andere verschijnselen zijn afhankelijk van eventuele aantasting van bloedvaten of zenuwen in de liquorruimte, dan kunnen oogbewegingen gestoord zijn of kan een lichaamshelft verlamd zijn. Aantasting van bloedvaten of zenuwen in de cochlea kan het kind doof maken. Van de kinderen tussen nul en tien jaar met bacteriële meningitis overleed tot enige jaren geleden 2.5% (Koomen, 2003; zie ook Roos, 1997).
Medische behandeling in de acute fase
Het kind wordt behandeld met antibiotica om de ziekteverwekker te bestrijden. Om het risico op gehoorverlies en neurologische gevolgen te verminderen worden corticosteroïden toegediend (Brouwer et al., 2013). Afhankelijk van de gevoeligheid van de ziekteverwekker kan het verstrekte antibioticum verschillen. Zo nodig worden anti-epileptica gegeven om epileptische aanvallen tegen te gaan.
Restverschijnselen en hun behandeling
Blijvend gehoorverlies doet zich voor bij ongeveer zeven procent van de kinderen, zwakzinnigheid bij twee procent en epilepsie ook bij twee procent (ENCYCL-Zwakzinnigheid). Drie andere restverschijnselen zijn elk bij ongeveer 1 procent of minder vastgesteld: hydrocefalus door verkleving van hersenvliezen en belemmering van de liquorcirculatie, verlamming in een lichaamshelft door een infarct en gezichtsveldbeperking ook door een infarct (Koomen, 2003). De percentages zijn lager dan veelal gerapporteerd, mogelijk door medebehandeling met corticosteroïden.
Bij ernstig gehoorverlies en verbindweefseling van de cochlea moet plaatsing van een cochleair implantaat worden overwogen, epilepsie kan noodzaken tot langdurige behandeling met geneesmiddelen (zie Ziektebeschrijving Epilepsie) en hydrocefalus tot het aanbrengen van een kunstmatige afvoer van liquor (zie Ziektebeschrijving Hydrocefalus ) (Koomen, 2003; Koomen et al., 2003; Merkus et al., 2007; Jennekens-Schinkel & Jennekens 2008).
Stoornissen van het cognitieve functioneren
Stoornissen van het cognitieve functionerenMentale ontwikkeling en intelligentie
Kinderen die zonder restverschijnselen herstellen van meningitis hebben als groep op schoolleeftijd geen duidelijk lager intelligentie quotiënt (IQ) dan kinderen van overeenkomstige leeftijd die geen hersenvliesontsteking of andere neurologische ziekte hebben gehad. Verbaal en performaal IQ verschillen niet.
Bij kinderen met neurologische restverschijnselen voltrekt de mentale ontwikkeling zich minder vlot dan bij kinderen zonder neurologische complicaties en is het risico van zwakzinnigheid (IQ < 70) wat groter dan normaal (Koomen et al., 2004; Taylor et al., 2000).
Andere cognitieve functies
Vier tot tien jaren na hun genezing van meningitis functioneren de kinderen merendeels normaal. Een lichte globale achterstand komt voor, vaak in samenhang met lichte motorische onrijpheid (Koomen et al., 2004).
Schoolvaardigheden: lezen, schrijven, rekenen
Van de Nederlandse kinderen die jaren geleden genazen van meningitis beheerst een kleine meerderheid (63%) rekenen, lezen en spellen op leeftijdsniveau. De anderen hebben een generiek, in alle belangrijke schoolvakken blijkend, leerprobleem (Koomen et al., 2004).
Psychosociaal functioneren
Psychosociaal functionerenSchoolloopbaan
Dertig procent van de Nederlandse kinderen zonder restverschijnselen van de doorgemaakte meningitis, doubleert een klas. Dat is veel meer dan normaal (in de overeenkomstige periode voor de gehele schoolgaande populatie ongeveer 11%). Dertien procent van de kinderen is geplaatst op scholen voor speciaal onderwijs, ook aanmerkelijk meer dan normaal (5%) (Koomen et al., 2004).
Gedrag
Kort na meningitis kunnen klachten bestaan over ongedurigheid of andere gedragsveranderingen, maar deze verdwijnen mettertijd. Op de lange duur komen gedragsproblemen niet meer voor dan bij andere kinderen (Ritchie et al., 2008).
Kwaliteit van leven
Kwaliteit van levenNederlandse ouders beoordelen de met gezondheid samenhangende kwaliteit van leven van hun kinderen na meningitis als kwetsbaarder dan Nederlandse ouders van andere kinderen (Koomen et al., 2005).
Begeleiding
BegeleidingMeningitis is een ernstige ziekte die kind en ouders plotseling, als een dief in de nacht, overvalt.
Onderzoek naar gehoorverlies behoort al plaats te vinden in de herstelfase van de meningitis voordat ontslag uit het ziekenhuis plaats vindt. Zo nodig moet dan snel een cochleair implantaat worden aangebracht waarna begeleiding plaats vindt in een audiologisch centrum. Te zijner tijd kan geadviseerd worden over schoolplaatsing, ingeval van hardhorendheid of doofheid bij voorkeur in Cluster 2 (voor kinderen met een auditieve handicap).
In de Ziektebeschrijvingen Epilepsie, Beroerte en Hydrocefalus wordt de begeleiding beschreven van kinderen die epileptische aanvallen houden, die uitvalsverschijnselen hebben ten gevolge van een herseninfarct of die hydrocefalus hebben door een liquorcirculatiestoornis.
Voor de vraag waarom zoveel kinderen na meningitis problemen hebben op school is tot nu toe geen goed antwoord. In het Nederlandse onderzoek waren geheel doof geworden kinderen niet meegenomen, maar 10% van de groep had meetbaar gehoorverlies en 17% had motorische rijpingsachterstand. Beide factoren kunnen een rol gespeeld hebben bij de beslissing tot laten doubleren of overplaatsen van de kinderen. Voorts kan niet uitgesloten worden dat het gevoel dat het kind sinds de meningitis fysiek kwetsbaarder is de betrokkenen gemakkelijker doet besluiten tot plaatsing op scholen voor speciaal onderwijs. Advisering door een (neuro)psycholoog met kennis van de gevolgen van meningitis kan voorbarig overplaatsen voorkomen.
Een kind met bacteriële meningitis
Een kind met bacteriële meningitis fajenn 3 juli, 2010 - 20:38Literatuur
LiteratuurBrouwer MC, McIntyre P, Prasad K, van de Beek D (2013) Corticosteroids for acute bacterial meningitis. Cochrane Database Systematic Review 6: CD004405
Jennekens-Schinkel A & Jennekens FGI (2008) Neuropsychologie van neurologische aandoeningen in de kindertijd. Amsterdam: Uitgeverij Boom, Hoofdstuk 5
Koomen I, Grobbee DE, Roord JJ, Donders R, Jennekens-Schinkel A, Furth AM van (2003) Hearing loss at school age in survivors of bacterial meningitis: assessment, incidence and prediction. Pediatrics 112: 1049-1053
Koomen I (2003) Prognosis of bacterial meningitis in childhood. Proefschrift Universiteit Utrecht. Utrecht: Labor Grafimedia
Koomen I, Furth AM van, Kraak MAC, Grobbee DE, Roord DJ, Jennekens-Schinkel A (2004) Neuropsychology of academic and behavioral limitations in school-age survivors of bacterial meningitis. Developmental Medicine & Child Neurology 46: 724-732
Koomen I, Raat H, Jennekens-Schinkel A, Grobbee DE, Roord JJ, Furth M van (2005) Academic and behavioral limitations and health-related quaility of life in school-age survivors of bacterial meningitis. Quality of Life Research 14: 1563-1572
Merkus P, Furth AM van, Govaerts ST, Suèr M, Smit F (2007) Doofheid na bacteriële meningitis bij jonge kinderen: ingrijpen voor de cochlea is geoblitereerd. Nederlands Tijdschrift voor Geneeskunde 151: 1209-1213
Ritchie L, Jennekens-Schinkel A, van Schooneveld M, Koomen I en Geenen R (2008) Surviving meningitis in childhood; behaviour is not really at risk. Acta Pædiatrica 97: 438-441
Roos KL (1997) Bacterial meningitis. In: Roos KL (editor) Central Nervous System Infectious Diseases and Therapy. New York: Marcel Dekker Inc, Chapter 5, pp 99-126
Taylor HG, Schatschneider C, Minich NM (2000) Longitudinal outcomes of haemophilus influenzae meningitis in school-age children. Neuropsychology 14: 509-518
Metachromatische leukodystrofie
Metachromatische leukodystrofie fajenn 6 februari, 2011 - 15:35Inleiding
InleidingMetachromatische leukodystrofie (MLD) is een stapelingsziekte, een van de vele zeldzame erfelijke stoornissen van de stofwisseling. Door tekort aan activiteit van een enzym hoopt zich een afbraakproduct in het weefsel op. Bij kleuring van zenuwweefsel voor microscopisch onderzoek (zoals vroeger gebruikelijk voor diagnostiek) blijkt het afbraakproduct een andere kleur te hebben dan de omgevende structuren. Dat verklaart de term metachromatisch (anderskleurig). Men spreekt van leukodystrofie omdat het vooral een aandoening is van de witte stof in het zenuwweefsel. Van lang niet alle erfelijke stofwisselingsziekten zijn neuropsychologische gegevens beschikbaar. In beperkte mate is dat wel het geval bij MLD.
Na enkele inleidende paragrafen zal eerst een korte samenvatting van de lichamelijke verschijnselen, van de huidige diagnostiek en van de therapie worden geboden waarna nader zal worden ingegaan op cognitieve en gedragsmatige aspecten. De tekst wordt afgesloten met een ziektegeschiedenis.
Andere teksten op internet
Andere teksten op internetwww.kinderneurologie.eu: biedt een uitvoerige Nederlandstalige beschrijving van het ziektebeeld door een kinderneuroloog.
www.ncbi.nlm.nih.gov/OMIM: De Engelstalige site over erfelijke ziekten van de John Hopkins Universiteit in de VS.
www.stofwisselingsziekten.nl: een fraai verzorgde Nederlandstalige site waarin ook MLD aan de orde komt.
Epidemiologie
EpidemiologieUit studies in de VS en Nederland blijkt dat de prevalentie bij geboorte tussen 1 en 1.5 per 100.000 bedraagt (Bonkowski et al., 2010; Poorthuis et al., 1999). In genetisch geïsoleerde groepen mensen worden veel hogere prevalenties aangetroffen.
Erfelijkheid en genmutatie
Erfelijkheid en genmutatieDe ziekte is autosomaal recessief erfelijk.
- In de grote meerderheid der gevallen wordt de ziekte veroorzaakt door een mutatie in het gen dat de code bevat van het enzym arylsulfatase A op chromosoom 22. Als beide ouders een gemuteerd arylsulfatase A gen dragen heeft ieder van hun kinderen een kans van 25% op MLD. Er zijn veel verschillende mutaties van het arylsulfatase A gen bekend.
- Het arylsulfatase A is nodig voor de afbraak van een sulfatide verbinding. De sulfatide verbinding moet gemobiliseerd worden, beschikbaar gemaakt, wil afbraak kunnen plaats vinden. Voor de mobilisatie is een activator (saponine B) nodig. Ontbreekt deze, dan kan MLD het resultaat zijn (Gieselmann en Krägeloh-Mann, 2010).
Oorzaak
OorzaakArylsulfatase A is een lysosomaal enzym. Ontbreekt arylsulfatase A of is er een deficiëntie of ontbreekt saponine B dan hoopt het niet afgebroken chemisch product op in de lysosomen van oligodendrogliacellen en Schwanncellen, en in enige mate in zenuwcellen. Oligodendroglia en Schwanncellen zijn betrokken bij de aanmaak van myeline in het centrale- respectievelijk perifere zenuwstelsel. Wordt er al teveel gestapeld dan volgt afbraak van het myeline, dat wil zeggen van witte stof. Hoe de stapeling myeline afbraak (demyelinisatie) tot gevolg kan hebben is niet bekend. De ziekteverschijnselen van MLD worden geheel of vrijwel geheel toegeschreven aan de demyelinisatie. De ernst hangt af van de mutaties. Soms ontbreekt activiteit van arylsulfatase A geheel, soms is er nog restactiviteit (Gieselmann-Krägeloh-Mann, 2010).
Lichamelijke verschijnselen
Lichamelijke verschijnselenEnigszins schematiserend worden drie vormen van de ziekte onderscheiden (Gieselmann & Krãgeloh-Mann, 2010; Jennekens-Schinkel & Jennekens, 2008).
Laat infantiele vorm
Bijna de helft van alle gevallen van MLD behoort tot deze vorm. De eerste verschijnselen treden meestal op in de loop van het tweede levensjaar, in ieder geval voor de leeftijd van 3 jaar (vanaf negende tot 27ste maand bij 21 kinderen; Kehrer et al., 2011). Het beeld begint met symptomen die passen bij een aandoening van het perifere zenuwstelsel: de kinderen leren wel lopen maar de spieren worden slap en verzwakken, het lopen gaat snel achteruit en de peesreflexen verdwijnen. Later worden de spieren stijf en atrofisch, er ontstaan pathologische reflexen, het kind kan niet meer zitten, de spraak wordt dysartrisch, het contact vermindert. Blindheid, aanvallen van epilepsie en strekkrampen (verschijnselen van motorische ontremming) komen voor. De kinderen overlijden vaak omstreeks het 6de levensjaar, maar het beloop kan ook korter of veel langer zijn.
Juveniele vorm
In 30-40% van de ziektegevallen past het beloop bij de juveniele vorm. De eerste verschijnselen ontstaan tussen het tweede tot derde en 16de jaar (bij 38 kinderen tussen 3 en 14 jaar; Kehrer et al., 2011). Symptomen van het perifere zenuwstelsel ontbreken of staan op de achtergrond. Leer- en gedragsstoornissen kunnen de beginverschijnselen zijn. Het ziektebeloop is langzamer dan bij de laat infantiele vorm; de ziekteduur kan wel twintig jaar bedragen.
Adulte vorm
De ziekte presenteert zich in het algemeen met gedragsveranderingen, cognitieve stoornissen, psychose of epilepsie. In de loop van tientallen van jaren verergert het beeld zeer geleidelijk.
Diagnose
DiagnoseDe demyelinisatie van perifere zenuwen wordt meestal ontdekt bij onderzoek van hun geleidingssnelheid. De aantasting van het myeline (witte stof) in de hersenen blijkt bij MRI. In de urine wordt de abnormale uitscheiding van sulfatiden aangetoond en in het bloed de enzymdeficiëntie. De genmutatie kan door DNA-onderzoek worden aangetoond. Kinderen bij wie de ziekte zich presenteert met veranderingen van cognitie en gedrag worden vaak pas na geruime tijd goed gediagnosticeerd. In de tussentijd kunnen tal van vergissingen worden gemaakt in interpretatie en behandeling van de gedragsveranderingen.
Medische behandeling en preventie
Medische behandeling en preventieVoor zover de ziekte kan worden tegengegaan, gebeurt dat door hematopoëtische stamcel transplantatie (zie ook ENCYCL-hematopoëtische stamcel transplantatie). Bij deze behandeling ontwikkelen cellen met het intacte gen afkomstig van het beenmerg zich in het centrale zenuwstelsel tot microglia. Geruime tijd verstrijkt voordat deze microglia effectief is. Eenmaal ontstane afwijkingen herstellen niet of onvoldoende, progressie kan worden tegengegaan. Voor de laat infantiele vorm kost dit therapieproces teveel tijd. Onderzoek over het therapeutisch nut van enzymtoediening of van gentherapie is gaande (Gieselmann & Krägeloh-Mann, 2010; Pierson et al., 2008).
Voor tal van symptomen (ziekteverschijnselen) is behandeling wel mogelijk, bijvoorbeeld voor pijn, spasmen, psychose, epilepsie.
Preventie van de ziekte is mogelijk door vruchtwateronderzoek in het begin van de zwangerschap en zo nodig abortus.
Cognitie en gedrag
Cognitie en gedragHet cognitieve verval verloopt met verschillende snelheid, niet alleen bij de diverse vormen van de ziekte maar ook bij vergelijking van twee aangedane kinderen met dezelfde genetische afwijking in een gezin. De organische basis van aandachtstoornissen en gedragsproblemen wordt in de aanvangsfase vaak langdurig miskend.
In onderstaande figuur zijn bevindingen weergegeven van cognitief en motorisch testonderzoek van 21 kinderen (leeftijd tussen 2 en 7 jaar) die verkeerden in de diagnostische fase van de ziekte. Allen hadden beginsymptomen voor de leeftijd van 6 jaar. De cognitieve domeinen (auditief verwerken, waarnemen, taal, verbaal geheugen en visueel geheugen) werden onderzocht met verschillende, maar leeftijdsadequate gestandaardiseerde tests. Voor onderlinge vergelijkbaarheid van de test uitslagen werden de scores getransformeerd in z-scores (gemiddeld = 0, standaarddeviatie = 1. Alle gemiddelden liggen onder het normgemiddelde, de spreiding is in alle domeinen fors, de motoriek is het meest gestoord. Beperkte woordenschat, overmatig zoeken naar woorden, gebruik van lege woorden en wijdlopigheid kenmerken het mondelinge taalgebruik. Echte afasie komt zelden of niet voor.
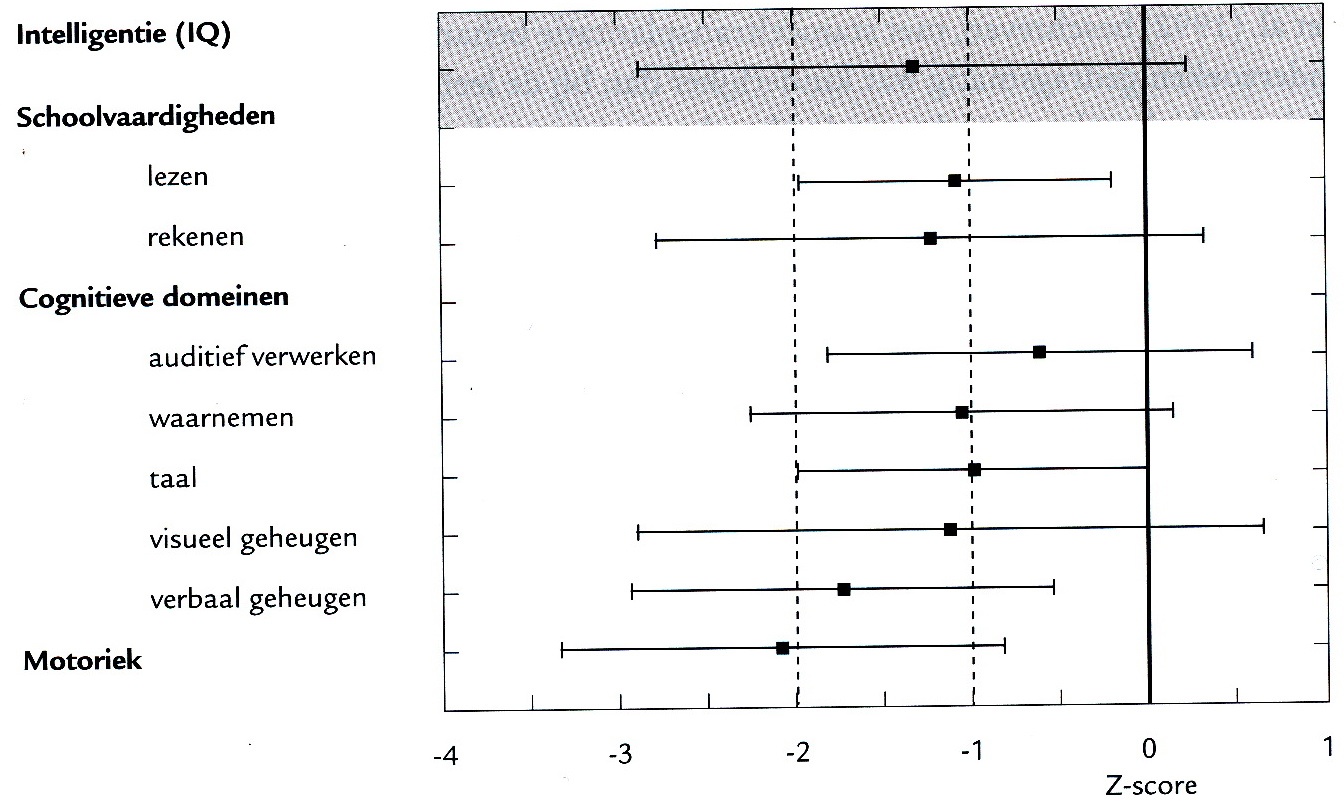
Begeleiding
Begeleiding- Diagnostische en therapeutische onzekerheid zijn moeilijk te verwerken, dat geven zowel ouders als zieke kinderen aan.
- Ouders en zusjes of broers behoeven bijstand en informatie over het te verwachten ziektebeloop - ook ten aanzien van cognitie en gedrag - en de moeilijkheden die zich daarbij kunnen voordoen.
- Het zieke kind dient zo lang en zoveel mogelijk zelfstandig te functioneren.
Een kind met metachromatische leukodystrofie
Een kind met metachromatische leukodystrofieJob was tot omstreeks zijn 9e jaar een opgewekte, sociaal ingestelde jongen. Op school was hij tot groep 6 een goede leerling. Hij veranderde echter. Hij kreeg conflicten, ging in bed plassen en presteerde steeds minder op school. (Figuur 2 toont beloop van leervorderingen en gedrag.) Voor dat alles was geen oorzaak aanwijsbaar. Zijn ouders merkten dat hij veel op zijn tenen liep en sleepte met een been. Aanvankelijk werden de diagnoses PDD-NOS en syndroom van Rett overwogen. MLD werd gediagnosticeerd toen hij 10 jaar was. Ouders en brusjes waren gezond; de ouders hadden een hogere opleiding genoten en werkten dienovereenkomstig.
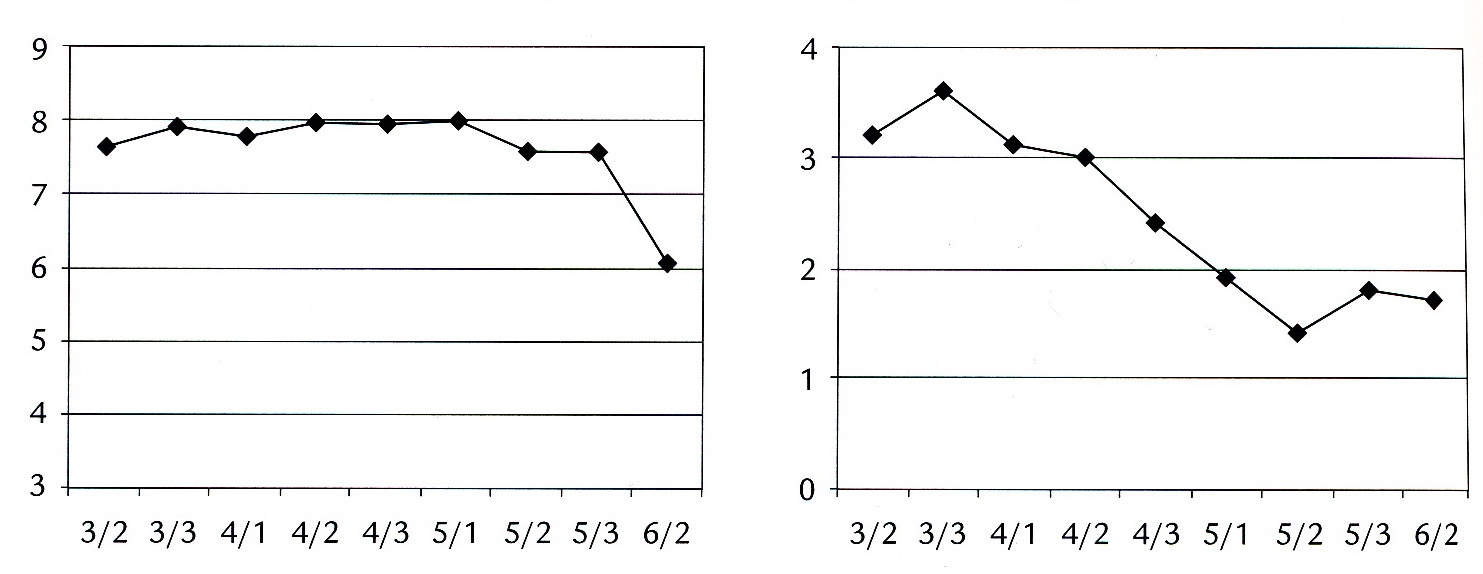
Neuropsychologisch onderzoek
Job werd voor het eerst neuropsychologisch onderzocht toen hij 10 jaar was, tenminste 2 jaar na de eerste verschijnselen van de ziekte.
- Gedrag bij onderzoek: stille jongen die goed meewerkt. Aandacht en concentratie zijn duidelijk gestoord. Ten tijde van het onderzoek plast hij in zijn broek.
- Intelligentie: Totaal intelligentiequotiënt (TIQ) = 52, Verbaal IQ = 57, Performaal IQ = 51 (Wechsler Intelligence Scale for Children-Revised).
- Geheugen: Geringe onmiddellijke geheugenspanne voor auditief aangeboden cijfers en voor visueel aangeboden sequenties, passend bij het IQ. In een leertaak (Locaties leren) is het begin zwak en ontstaat hoegenaamd geen leereffect. Bij navertellen van een verhaal confabuleert Job.
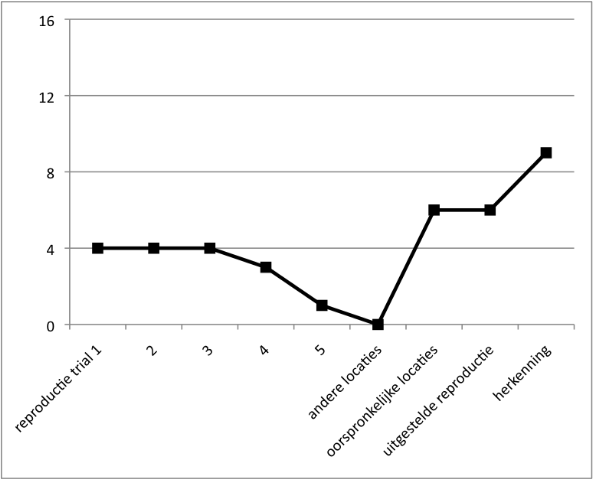
Figuur 3. Locaties leren. - Spraak en taal: De spraak is traag en moeilijk verstaanbaar. Job gebruikt veel stereotype frasen. Hij heeft moeite met vinden van woorden, zo blijkt ook bij benoemen van afbeeldingen. In een zinnendictee maakt Job veel controlefouten. (zie Figuur 4a en b). Bij hardop lezen raakt hij de regel kwijt en slaat hij woorden over.

Gedicteerd tijdens onderzoek: vader moet zich nog scheren - soep zonder zout smaakt flauw - welke vruchten eten wij in de winter? - Eva knoeit wel erg met de inkt.

- Rekenen: Bij schriftelijk rekenen lukt optellen slecht en aftrekken erg slecht.
- Grafisch construeren: het vroeger regelmatige handschrift is chaotisch geworden (zie figuur 3); de ooit rijke, fantasievolle tekeningen zijn nu pover.
- Gedragsregulatie: Job kan sorteren maar van sorteerprincipe wisselen lukt niet zonder begeleiding.
- Lichaamschema: intact.
- Reactiesnelheid: Job begrijpt de instructie niet en heeft onvoldoende aandacht voor de taak.
- Handvastheid en handvaardigheid : Bij uitvoeren van taken trillen de handen soms heftig. Coördinatie en differentiatie van het bewegen zijn gestoord.
Laboratoriumonderzoek
Bij enzymonderzoek blijkt arylsulfatase A deficiëntie. De sulfatidefractie in de urine is verhoogd. Bij beeldvorming (MRI) blijken beiderzijds in de witte stof van de hersenen grote confluerende afwijkingen (zie Figuur 5)
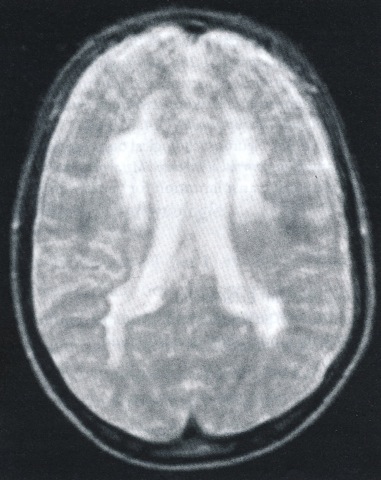
Transversale (dwars, horizontaal)MRI-opname (T2). Het beeld is onscherp door bewegen tijdens het onderzoek. De uitgebreide witte stof afwijkingen beiderzijds in het gebied nabij de hersenkamers zijn duidelijk zichtbaar
Beleid
Omdat de cognitieve stoornissen al ernstig zijn wordt afgezien van stamceltransplantatie. De behandeling is symptomatisch.
Literatuur
LiteratuurBonkowski JL, Nelson C, Kingston JL, Filloux FM, Mundorff MB, Srivastava V (2010) The burden of inherited leukodystrophies. Neurology 75: 718-725
Gieselmann V, Krägeloh-Mann L (2010) Metachromatic leukodystrophy-An update. Neuropediatrics 41: 1-6
Jennekens-Schinkel A, Jennekens FGI (2008) Neuropsychologie van neurologische aandoeningen in de kindertijd. Amsterdam: Boom, pp 562-574
Kehrer C, Blumenstock G, Raabe C, Krägeloh-Mann I (2011) Development and reliability of a classification system for gross motor function in children with metachromatic leukodystrophy. Developmental Medicine & Child Neurology 53: 156-160
Pierson M, Bonnemann CG, Finkel RS, Bunin N, Tennekom GI (2008) Umbilical cord blood transplantation for juvenile metachromatic leukodystrophy. Annals of Neurology 64: 583-587
Poorthuis BJHM, Wevers RA, Kleijer WJ, Groener JEM, de Jong JGN, van Weely S, Niezen-Koning KE, Diggelen OP (1999) The frequency of lysosomal storage diseases in the Netherlands. Human Genetics 105: 151-156
Shapiro EG, Lockman LA, Bathazor M, Krivit W (1995) Neuropsychological outcomes of several storage diseases with and without bone marrow transplantation. Journal of Inherited Metabolic Diseases 18: 413-429